Чтобы изотермически уменьшить объем газа в цилиндре с поршнем в n раз
Обновлено: 05.07.2024
Какое количество тепла необходимо сообщить азоту при его изобарическом нагревании, чтобы газ совершил работу $A = 2,0 Дж$?
Задача по физике - 7073
Один моль некоторого идеального газа изобарически нагрели на $\Delta T = 72 К$, сообщив ему количество тепла $Q = 1,60 кДж$. Найти совершенную газом работу, приращение его внутренней энергии и величину $\gamma = C_/C_$.
Задача по физике - 7074
Два моля идеального газа при температуре $T_ <0>= 300 К$ охладили изохорически, вследствие чего его давление уменьшилось в $n = 2,0$ раза. Затем газ изобарически расширили так, что в конечном состоянии его температура стала равной первоначальной. Найти количество тепла, поглощенного газом в данном процессе.
Задача по физике - 7075
Вычислить величину $\gamma = C_/C_$ для газовой смеси, состоящей из $\nu_ = 2,0$ моля кислорода $\nu_ = 3,0$ моля углекислого газа. Газы считать идеальными.
Задача по физике - 7076
Вычислить удельные теплоемкости $c_$ для газовой смеси, состоящей из 7,0 г азота и 20 г аргона. Газы считать идеальными.
Задача по физике - 7077
В вертикальном цилиндре под поршнем находится один моль некоторого идеального газа при температуре $T$. Пространство над поршнем сообщается с атмосферой. Какую работу необходимо совершить, чтобы, медленно поднимая поршень, изотермически увеличить объем газа под ним в $n$ раз? Трение поршня о стенки цилиндра пренебрежимо мало.
Задача по физике - 7078
Внутри закрытого с обоих концов горизонтального цилиндра находится легкоподвижный поршень. Первоначально поршень делит цилиндр на две равные части, каждая объемом $V_<0>$, в которых находится идеальный газ одинаковой температуры и под одним и тем же давлением $p_<0>$. Какую работу необходимо совершить, чтобы, медленно двигая поршень, изотермически увеличить объем одной части газа в $\eta$ раз по сравнению с объемом другой части?
Задача по физике - 7079
Три моля идеального газа, находившегося при температуре $T_ <0>= 273 К$, изотермически расширили в $n = 5,0$ раза и затем изохорически нагрели так, что в конечном состоянии его давление стало равным первоначальному. За весь процесс газу сообщили количество тепла $Q = 80 кДж$. Найти величину $\gamma = C_/C_$ для этого газа.
Задача по физике - 7080
Изобразить для идеального газа примерные графики изо-хорического, изобарического, изотермического и адиабатического процессов на диаграмме:
а) $p, T$; б) $V, T$.
Задача по физике - 7081
Один моль кислорода, находившегося при температуре $T_ <0>= 290 К$, адиабатически сжали так, что его давление возросло в $\eta = 10,0$ раза. Найти:
а) температуру газа после сжатия;
б) работу, которая была совершена над газом.
Задача по физике - 7082
Некоторую массу азота сжали в $\eta = 5,0$ раза (по объему) один раз адиабатически, другой раз изотермически. Начальное состояние газа в обоих случаях одинаково. Найти отношение соответствующих работ, затраченных на сжатие.
Задача по физике - 7083
Внутри закрытого теплоизолированного цилиндра с идеальным газом находится легкоподвижный теплопроводящий поршень. При равновесии поршень делит цилиндр на две равные части и температура газа равна $T_<0>$. Поршень начали медленно перемещать. Найти температуру газа как функцию отношения $\eta$ объема большей части к объему меньшей Части. Показатель адиабаты газа $\gamma$.
Задача по физике - 7084
Определить скорость $v$ истечения гелия из теплоизолированного сосуда в вакуум через малое отверстие. Считать, что при этом условии скорость потока газа в сосуде пренебрежимо мала. Температура гелия в сосуде $T = 1000 К$.
Задача по физике - 7085
Объем идеального газа с показателем адиабаты $\gamma$ изменяют по закону $V = a/T$, где $a$ — постоянная. Найти количество тепла, полученное одним молем газа в этом процессе, если температура газа испытала приращение $\Delta T$.
Задача по физике - 7086
Показать, что процесс, при котором работа идеального газа пропорциональна соответствующему приращению его внутренней энергии, описывается уравнением $pV^ < n>= const$, где $n$ — постоянная.

Задание 10 № 7141
Относительная влажность воздуха в цилиндре под поршнем равна 70 %. Воздух изотермически сжали, уменьшив его объём в два раза. Какова стала относительная влажность воздуха? (Ответ дайте в процентах.)
Относительной влажностью называют отношение давления пара к давлению насыщенного пара при той же температуре. В силу того, что пар можно описывать при помощи уравнения для идеального газа: Для относительной влажности имеем:
Если объем газа уменьшить в 2 раза, его концентрация возрастет в 2 раза. Следовательно, относительная влажность также увеличится в 2 раза. Но, при достижении относительной влажности в 100 %, изменение объема никак не влияет на значение этой относительной влажности. Строго говоря, относительная влажность не может быть больше 100 % (из условий задачи — ).


изопроцессы
12/14/21

Изопроцессы
макропараметры?
ИЗОПРОЦЕССЫ
Процесс, протекающий при одном постоянном макропараметре, называется изопроцессом
макропараметре
Изопроцессы

Изотермический процесс
Закон Бойля-Мариотта
Закон Бойля-Мариотта
Изотермическиq процесс – процесс изменения состояния давления и объема определенной массы газы при постоянной температуре.
При изотермическом процессе
Т=const

Закон Бойля-Мариотта
Для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
pV = const
p 1 V 1 = p 2 V 2

Закон Бойля-Мариотта
При постоянной температуре давление данной массы газа обратно пропорционально его объёму.
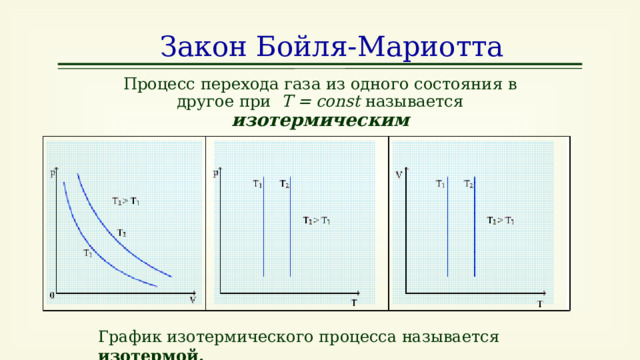
Процесс перехода газа из одного состояния в другое при Т = const называется изотермическим
График изотермического процесса называется изотермой.

Закон получен экспериментально
Закон Гей - Люссака
Изобарный процесс
Жозеф Луи Гей-Люссак

Закон Гей - Люссака
Изобарный процесс – процесс изменения состояния определенной массы газы при постоянном давлении .
р = const

Закон Гей - Люссака
При посеянном давлении объем данной массы газа прямо пропорционален температуре.

Закон Гей - Люссака
Чем отличаются две эти формулы
Объем данной массы газа при постоянном давлении линейно изменяется с температурой.
Разная шкала температур.
V 0 - объем, занимаемый газом
при температуре 0 °С;
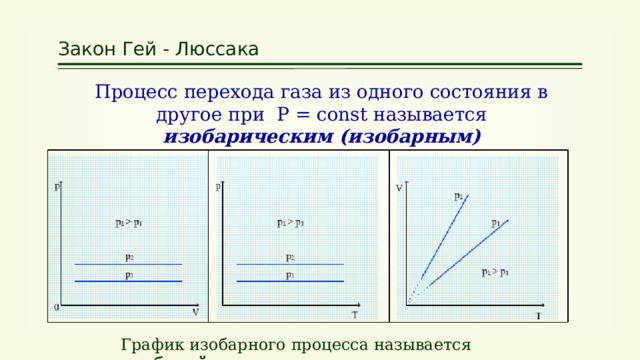
Закон Гей - Люссака
Процесс перехода газа из одного состояния в другое при Р = const называется изобарическим (изобарным)
График изобарного процесса называется изобарой.

Закон получен экспериментально
Закон Шарля
Изохорный процесс
Ж ак Александр Сезар Шарль
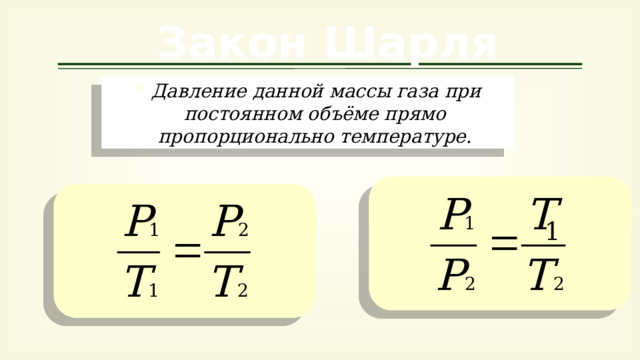
Закон Шарля
Закон Шарля
- Давление данной массы газа при постоянном объёме изменяется с температурой линейно.
Р 0 - давление газа при температуре 0 °С;
α – температурный коэффициент давления
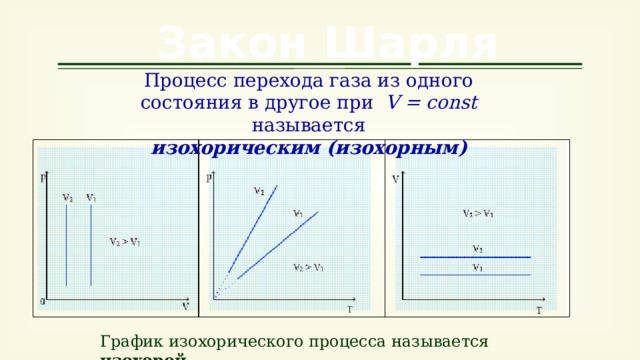
Закон Шарля
Процесс перехода газа из одного состояния в другое при V = const называется изохорическим (изохорным)
График изохорического процесса называется изохорой.
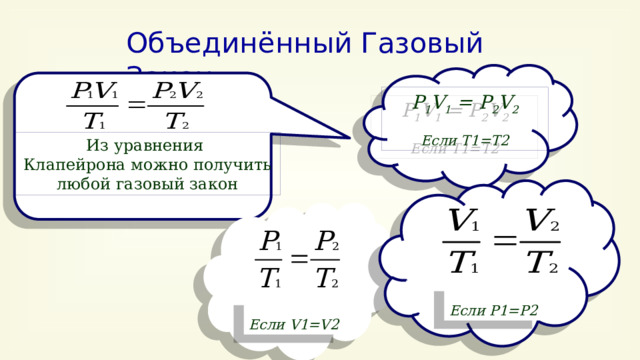
Объединённый Газовый Закон
P 1 V 1 = P 2 V 2
Клапейрона можно получить любой газовый закон

- Вопрос 1. Во сколько раз увеличится объем воздушного шара, если его внести с улицы в теплое помещение? Температура на улице -30С, в помещении +270С.
- Вопрос 2. Чтобы изотермически уменьшить объема газа в цилиндре с поршнем в 3 раза, на поршень поместили груз 9 кг. Какой дополнительный груз (кг) следует поместить на поршень, чтобы объем газа изотермически уменьшить еще в 2 раза?
- Вопрос 3. Сосуд с газом плотно закрыт пробкой, площадь сечения которой 2,5 см2. Сила трения, удерживающая пробку, равна 12 Н. Начальное давление в сосуде 100 кПа, температура 270 К. Сосуд нагревают. Определите температуру (К), до которой нужно нагреть газ в сосуде, чтобы пробка вылетела.
Циклический процесс
Процесс перехода газа из одного состояния в другие, когда конечное состояние совпадает с начальным

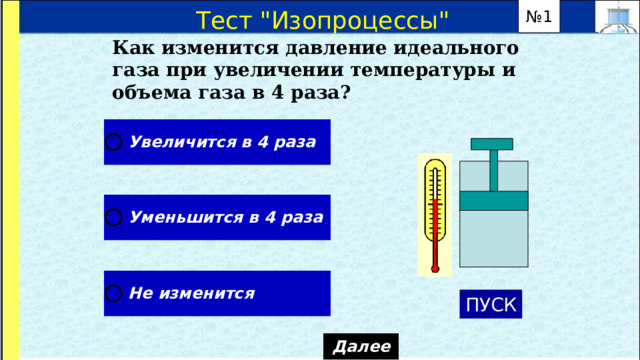
Как изменится давление идеального газа при увеличении температуры и объема газа в 4 раза?
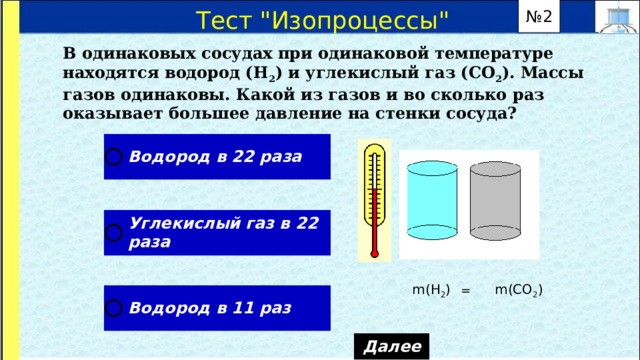
В одинаковых сосудах при одинаковой температуре находятся водород (Н 2 ) и углекислый газ (СО 2 ). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки сосуда?
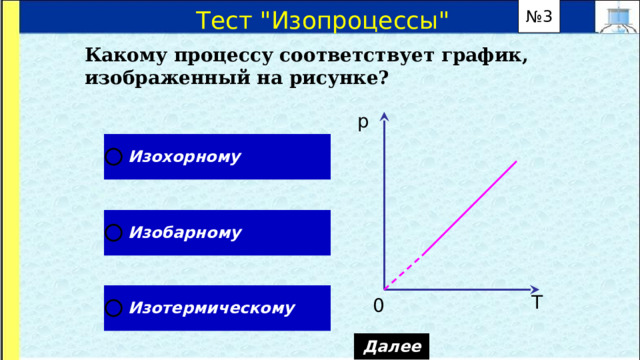
Какому процессу соответствует график, изображенный на рисунке?
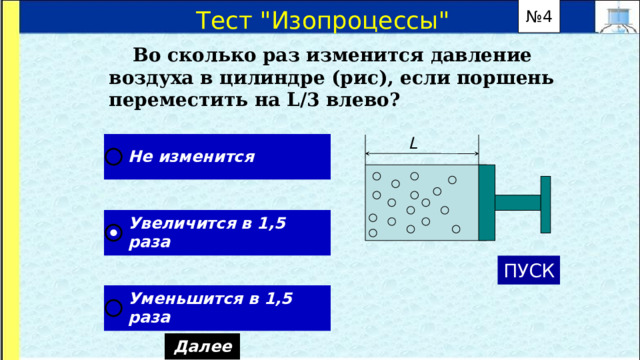
Во сколько раз изменится давление воздуха в цилиндре (рис), если поршень переместить на L/3 влево?
Во сколько раз отличается плотность метана (СН 4 ) от плотности кислорода (О 2 ) при одинаковых условиях ?
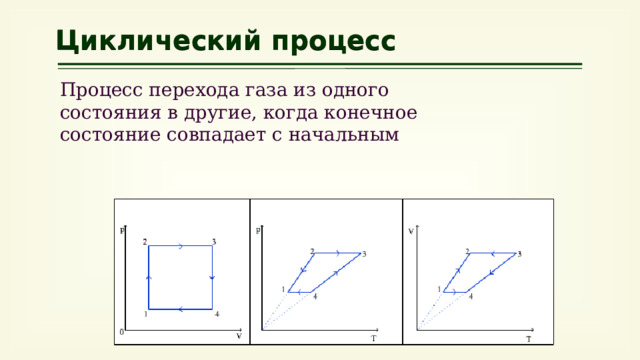
Циклический процесс
Процесс перехода газа из одного состояния в другие, когда конечное состояние совпадает с начальным

1. В сосуде емкостью 10 л находится метан массой 2 кг. Найдите давление метана на стенки сосуда, если его температура 15 °С.
2. Определите число молекул воздуха в комнате размерами 8х5х3 метра, при температуре 23 °С и давлении 10 5 Па.
3. Найдите плотность 5 л азота, находящегося под давлением 100 кПа, если средняя кинетическая энергия его молекул равна 1 нДж.

Знать уравнение состояния необходимо при исследовании тепловых явлений.
Оно позволяет полностью или частично ответить сразу на три группы различных вопросов:
- позволяет определить одну из величин, характеризующих состояние, если известны две другие величины
- можно сказать, как протекают в системе различные процессы при определенных внешних условиях
- можно определить, как меняется состояние системы, если она совершает работу или получает теплоту от окружающих тел.


изопроцессы
12/14/21

Изопроцессы
макропараметры?
ИЗОПРОЦЕССЫ
Процесс, протекающий при одном постоянном макропараметре, называется изопроцессом
макропараметре

Изопроцессы

Изотермический процесс
Закон Бойля-Мариотта
Закон Бойля-Мариотта
Изотермическиq процесс – процесс изменения состояния давления и объема определенной массы газы при постоянной температуре.
При изотермическом процессе
Т=const

Закон Бойля-Мариотта
Для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
pV = const
p 1 V 1 = p 2 V 2

Закон Бойля-Мариотта
При постоянной температуре давление данной массы газа обратно пропорционально его объёму.

Процесс перехода газа из одного состояния в другое при Т = const называется изотермическим
График изотермического процесса называется изотермой.

Закон получен экспериментально
Закон Гей - Люссака
Изобарный процесс
Жозеф Луи Гей-Люссак

Закон Гей - Люссака
Изобарный процесс – процесс изменения состояния определенной массы газы при постоянном давлении .
р = const

Закон Гей - Люссака
При посеянном давлении объем данной массы газа прямо пропорционален температуре.

Закон Гей - Люссака
Чем отличаются две эти формулы
Объем данной массы газа при постоянном давлении линейно изменяется с температурой.
Разная шкала температур.
V 0 - объем, занимаемый газом
при температуре 0 °С;

Закон Гей - Люссака
Процесс перехода газа из одного состояния в другое при Р = const называется изобарическим (изобарным)
График изобарного процесса называется изобарой.

Закон получен экспериментально
Закон Шарля
Изохорный процесс
Ж ак Александр Сезар Шарль

Закон Шарля
Закон Шарля
- Давление данной массы газа при постоянном объёме изменяется с температурой линейно.
Р 0 - давление газа при температуре 0 °С;
α – температурный коэффициент давления

Закон Шарля
Процесс перехода газа из одного состояния в другое при V = const называется изохорическим (изохорным)
График изохорического процесса называется изохорой.

Объединённый Газовый Закон
P 1 V 1 = P 2 V 2
Клапейрона можно получить любой газовый закон

- Вопрос 1. Во сколько раз увеличится объем воздушного шара, если его внести с улицы в теплое помещение? Температура на улице -30С, в помещении +270С.
- Вопрос 2. Чтобы изотермически уменьшить объема газа в цилиндре с поршнем в 3 раза, на поршень поместили груз 9 кг. Какой дополнительный груз (кг) следует поместить на поршень, чтобы объем газа изотермически уменьшить еще в 2 раза?
- Вопрос 3. Сосуд с газом плотно закрыт пробкой, площадь сечения которой 2,5 см2. Сила трения, удерживающая пробку, равна 12 Н. Начальное давление в сосуде 100 кПа, температура 270 К. Сосуд нагревают. Определите температуру (К), до которой нужно нагреть газ в сосуде, чтобы пробка вылетела.
Циклический процесс
Процесс перехода газа из одного состояния в другие, когда конечное состояние совпадает с начальным


Как изменится давление идеального газа при увеличении температуры и объема газа в 4 раза?

В одинаковых сосудах при одинаковой температуре находятся водород (Н 2 ) и углекислый газ (СО 2 ). Массы газов одинаковы. Какой из газов и во сколько раз оказывает большее давление на стенки сосуда?

Какому процессу соответствует график, изображенный на рисунке?

Во сколько раз изменится давление воздуха в цилиндре (рис), если поршень переместить на L/3 влево?

Во сколько раз отличается плотность метана (СН 4 ) от плотности кислорода (О 2 ) при одинаковых условиях ?

Циклический процесс
Процесс перехода газа из одного состояния в другие, когда конечное состояние совпадает с начальным

1. В сосуде емкостью 10 л находится метан массой 2 кг. Найдите давление метана на стенки сосуда, если его температура 15 °С.
2. Определите число молекул воздуха в комнате размерами 8х5х3 метра, при температуре 23 °С и давлении 10 5 Па.
3. Найдите плотность 5 л азота, находящегося под давлением 100 кПа, если средняя кинетическая энергия его молекул равна 1 нДж.

Знать уравнение состояния необходимо при исследовании тепловых явлений.
Оно позволяет полностью или частично ответить сразу на три группы различных вопросов:
- позволяет определить одну из величин, характеризующих состояние, если известны две другие величины
- можно сказать, как протекают в системе различные процессы при определенных внешних условиях
- можно определить, как меняется состояние системы, если она совершает работу или получает теплоту от окружающих тел.
Читайте также:

