Вертлужная впадина перелом последствия дтп
Обновлено: 16.05.2024
В статье проанализированы данные научной литературы по различным аспектам проблемы лечения пациентов с последствиями сложных переломов вертлужной впадины, проведена сравнительная оценка результатов лечения пациентов с данной патологией, пролеченных в РНИИТО им. Р.Р. Вредена, и выполнено математическое моделирование проведенных операций. Переломы вертлужной впадины являются наиболее сложным видом в структуре травмы костей таза и являются следствием высокоэнергетических воздействий, что обусловливает сочетанный и множественный характер повреждений у пострадавших, в результате чего своевременная диагностика и лечение переломов вертлужной впадины не всегда возможна. Наиболее часто встречающимся последствием переломов вертлужной впадины является прогрессирующее развитие деформирующего артроза тазобедренного сустава. Оптимальным функциональным методом восстановления поврежденного сустава является эндопротезирование тазобедренного сустава. Основной проблемой при выполнении артропластики в результате сложных переломов вертлужной впадины является достижение первичной стабильной фиксации ацетабулярного компонента, что связано с тяжелым нарушением анатомии вертлужной впадины, ее сферичности, наличием костных дефектов. Несмотря на большой перечень используемых методик и имеющихся современных имплантатов, частота осложнений и неудовлетворительных результатов хирургического лечения по-прежнему высока. В результате проведенного анализа выявлены наиболее перспективные методы артропластики тазобедренного сустава у пациентов с исследуемой патологией, позволяющие улучшить функциональный результат.

1. Giannoudis P.V., Bireher M., Pohlemann T. Advanses in pelvic and acetabulum surgery // Injury. - 2007. - № 38 (4). - С. 395-396.
2. Гудушаури Я.Г. Проблемные вопросы учения о политравме таза // Технологии живых систем. - 2016. - № 7. - С. 4-15.
3. Бесаев Г.М. Травматологические аспекты хирургической тактики лечения нестабильных повреждений таза в остром периоде травматической болезни / Г.М. Бесаев, В.Г. Багдасарьянц // Бюллетень Восточно-Сибирского научного центра СО РАМН. – 2007. - № 4. – 30 с.
4. Halawi M.J. Pelvic ring injuries: Emergency assessment and management // Journal of Clinical Orthopaedics and Trauma. – 2015. – 6 (4):252-258.
5. Kumar P., Sen R.K., Kumar V., Dadra A. Quality of life following total hip arthroplasty in patients with acetabular fractures, previously managed by open reduction and internal fixation // Chinese Journal of Traumatology. – 2016. – 19 (4):206-208.
6. Letournel E. Fractures of the acetabulum: a study of a series of 75 cases // J. Orthop Trauma. – 2006. - Jan; 20 (1 Suppl):S15-19.
7. Sen R.K. Posterior wall reconstruction using iliac crest strut graft in severely comminuted posterior acetabular wall fracture / R.K. Sen, S.K. Tripathy, S. Aggarwal, T. Tamuk // Int. Orthop. 2010. - Vol. 35, N 8. - P. 1223-1228.
8. Артюх В.А. Разработка усовершенствованных подходов к хирургическому лечению больных с переломами вертлужной впадины и их последствиями: автореф. дис. . канд. мед. наук: 14.00.22 / [Место защиты: Воен.-мед. акад. им. С.М. Кирова]. – СПб., 2007. - 23 с.: ил. РГБ ОД, 9 07-5/417.
9. Xie S., Manda K., Wallace R.J. et al. Time Dependent Behaviour of Trabecular Bone at Multiple Load Levels // Annals of Biomedical Engineering. – 2017. – 45 (5):1219-1226.
11. Тихилов P.M. Руководство по хирургии тазобедренного сустава / P.M. Тихилов, И.И. Шубняков. - СПб.: РНИИТО им. P.P. Вредена, 2015. - Т. II. – 85 с.
12. Morison Z., Moojen D.J.F., Nauth A. et al. Total Hip Arthroplasty After Acetabular Fracture Is Associated With Lower Survivorship and More Complications // Clinical Orthopaedics and Related Research. – 2016. – 474 (2):392-398.
13. Shin J.K. Analysis of Predictors of Results after Surgical Treatment of Acetabular Fractures / J.K. Shin, S.J. An, T.S. Go et al. // The Korean Hip Society (KAMJE). – 2015. – 27 (2):104.
15. Arola D., Bajaj D., Ivancik J. et al. Fatigue of Biomaterials: Hard Tissues // Int J Fat. – 2010. – 32 (9):1400–1412.
Переломы костеи? таза и вертлужнои? впадины составляют от 3 до 8% всех переломов скелета [1]. В структуре повреждений таза ацетабулярные переломы составляют от 7 до 20% [2]. В группе политравм эта цифра достигает 20%. На долю кататравм приходится 40% случаев тяжелых повреждений вертлужной впадины [3]. Основной причиной переломов вертлужной впадины являются дорожно-транспортные происшествия (90% случаев) [4].
За последнее столетие число пострадавших с тяжелыми переломами вертлужной впадины увеличилось почти в 20 раз [5]. Преобладающее большинство пациентов (до 73%) [6] с переломами вертлужной впадины - это трудоспособные, здоровые люди возраста моложе 50 лет, чаще мужчины. В связи с этим общество несет существенные социально-экономические потери, так как большинство пострадавших, по данным статистики, становятся стои?кими инвалидами или вынуждены сменить профессию [7]. К сожалению, в нашей стране большинству пострадавших с такими травмами проводится консервативное лечение [8], в то время как в ведущих зарубежных учреждениях выполняют открытую репозицию и фиксацию вертлужной впадины со смещением отломков у 70% пострадавших [9]. Стоит отметить, что восстановление конгруэнтности вертлужной впадины еще не гарантирует благоприятного исхода, так как возможны случаи несращения таких переломов. По данным литературы, неблагоприятные результаты, в зависимости от точности репозиции, могут достигать до 50%. А при тяжелых переломах, когда происходит центральный вывих головки бедренной кости, отрицательный результат близок к 90% [10].
По мнению современных исследователей, последствиями переломов вертлужной впадины являются прогрессирование болевого синдрома и нарушение функции нижней конечности. К неблагоприятным исходам как консервативного, так и оперативного лечения переломов вертлужной впадины относятся посттравматический артроз тазобедренного сустава, асептический некроз головки бедренной кости, гетеротопические оссификаты в области тазобедренного сустава, перелом металлоконструкций, являющиеся, по мнению многих исследователей, поздними осложнениями рассматриваемой патологии [11].
Несмотря на успешное выполнение открытой репозиции и внутренней фиксации переломов вертлужной впадины, 20% пострадавших нуждаются в дальнейшем хирургическом вмешательстве [12] в связи с развитием поздних осложнений или несращением переломов. Наиболее часто встречающимся последствием переломов впадины является прогрессирующее развитие деформирующего артроза тазобедренного сустава (30%) [13]. Появлению артроза способствуют не только травмы сами по себе, но и перенесенные по поводу них операции на суставе.
Даже учитывая современные подходы и возможности крупных ортопедических клиник, выбор метода оперативного лечения последствий тяжелого перелома вертлужной впадины ограничен артродезом и тотальным эндопротезированием тазобедренного сустава. Принцип артродеза тазобедренного сустава заключается в стабилизации сустава путем обеспечения его механической неподвижности, что совершенно невыгодно в функциональном отношении. В результате такой операции наступает декомпенсация со стороны пояснично-крестцового отдела позвоночника, коленного сустава.
В этой связи современными хирургами отдается предпочтение альтернативному методу функционального восстановления поврежденной конечности - тотальному эндопротезированию тазобедренного сустава с различными модификациями артропластики. Однако выполнение таких операций при последствиях тяжелых переломов вертлужной впадины - это трудоемкий процесс, который относится к операциям высокой сложности, обусловленный серьезными осложнениями, большой кровопотерей и продолжительной реабилитацией пострадавших после оперативного лечения. Также необходим высокий уровень подготовки хирурга, современное оснащение и наличие необходимых имплантов.
Анализ немногочисленных сведений специальной отечественной литературы о результатах эндопротезирования при тяжелых последствиях переломов вертлужной впадины определил актуальность данной темы научного исследования.
Цель исследования. Провести сравнительную оценку различных вариантов эндопротезирования тазобедренного сустава у пациентов с последствиями сложных переломов вертлужной впадины с нарушением целостности тазового кольца на основании математического моделирования таких операций и сравнительного анализа среднесрочных и отдаленных исходов лечения.
1 тип – отсутствие видимых нарушений костных структур и правильное их взаимоотношение в суставе. Может наблюдаться после переломов вертлужной впадины без смещения либо при достижении на предварительных этапах лечения идеальной анатомической репозиции. Укорочение конечности может наблюдаться только в случаях асептического некроза головки.
2 тип – наиболее часто встречающийся, является следствием повреждения задних отделов вертлужной впадины. В результате имеет место различной степени нарушение сферичности вертлужной впадины в сочетании с разнообразными дефектами задней стенки. Головка бедренной кости находится в состоянии подвывиха или вывиха. Учитывая значительную вариабельность по степени подвывиха головки и объема повреждения задних структур сустава, в этом типе выделяют 2а, 2б и 2в подтипы.
3 тип является проявлением тяжелых (как правило, ассоциированных) переломов, при которых нарушается непрерывность тазового кольца, которые в процессе лечения не были надлежащим образом репонированы и адекватно фиксированы.
В группу 1 были включены пациенты, у которых при тотальном эндопротезировании выполнялась фиксация ацетабулярного компонента винтами (не менее 4). К группе 2, в дополнение к ацетабулярному компоненту, фиксированному винтами, имплантировалась реконструктивная пластина. В 3-ю группу входили пациенты, которым выполнялось эндопротезирование поврежденного сустава с использованием антипротрузионного кольца Бурх-Шнайдера. В группу 4 были включены пациенты с последствиями переломов вертлужной впадины, при которых нарушалась ее сферичность, но не было разрыва тазового кольца. Период наблюдения за пациентами составил от 1 до 5 лет. Проведено анкетирование исследуемой когорты пациентов, оценены Rg-граммы в среднесрочном и отдаленном периодах, а также выполнен математический эксперимент на основе 3D-моделирования.
Результаты исследования и их обсуждение
Результаты статистической обработки данных показали, что в целом структура контингента - это молодые, физически активные, трудоспособные, чаще мужчины (71%), люди, которые в результате тяжелых травм могут стать инвалидами. Выявлены статистически значимые различия по продолжительности оперативного вмешательства, наименьшее время, затраченное на операцию, было у пациентов 2-й исследуемой группы. Однако разницы по продолжительности хирургических манипуляций в группах молодых и возрастных пациентов нет. Анализ кровопотери в разных возрастных группах, а также в зависимости от продолжительности операции статистически значимых различий не выявил. Хирургический доступ, используемый при лечении пациентов с исследуемой патологией, зависел в основном от предпочтений хирурга, который выполнял операцию. Однако удалось установить статистически значимое отличие. Так, при использовании заднего доступа (31%) продолжительность и кровопотеря у пациентов обеих возрастных групп значительно меньше, чем при использовании двух других доступов. Все это позволяет разрабатывать единые рекомендации по выбору тактики лечения этого контингента пациентов независимо от возраста и пола.
Проведенное анкетирование и оценка среднесрочных результатов лечения пациентов подтвердило отсутствие специфических жалоб или их комбинаций. Многофакторный анализ, проводившийся на основании данных международных шкал (Harris для оценки функционального состояния пациента, которому выполнялось тотальное эндопротезирование тазобедренного сустава, а также шкалы WOMAC и SF-36 для оценки психоэмоционального состояния), позволил составить суммарную картину среднесрочных результатов проведенного лечения. При этом усредненная оценка по оценочным шкалам показала различную степень достижения максимально возможного результата: Harris – 82, WOMAC-66, SF-36: PH- 48,672; MH- 57,036.
Проведенный сравнительный анализ ближайших и среднесрочных результатов лечения пациентов с последствиями сложных переломов вертлужной впадины с нарушением непрерывности тазового кольца с использованием 3 различных методик артропластики: 1 -установка и фиксация ацетабулярного компонента к костям таза винтами (не менее 4); 2 - дополнительно к вертлужному компоненту, фиксированному винтами, устанавливается реконструктивная пластина, соединяющая обе колонны таза; 3 - установка антипротрузионного кольца Бурх-Шнайдера с фиксацией его к костям таза винтами, позволил установить следующее. У пациентов после артропластики тазобедренного сустава с использованием трех вышеописанных методик на прослеженных этапах реабилитации (до 5 лет) значимой разницы функционального результата выявлено не было. Оценка ошибок и осложнений эндопротезирования тазобедренного сустава, приводящих к нестабильности ацетабулярного компонента эндопротеза тазобедренного сустава и необходимости ревизионного вмешательства, у пациентов с последствиями сложного перелома вертлужной впадины с нарушением непрерывности тазового кольца выявила высокую степень зависимости функционального результата от выбора хирургом способа фиксации ацетабулярного компонента во время оперативного вмешательства.
На основе изученного материала и проведенных экспериментов нами определено, что хорошие и отличные результаты эндопротезирования были достигнуты при всех 3 типах артропластики. Однако по результатам конечно-элементного расчета определены силы, действующие на каждый из винтов, фиксирующих ацетабулярный компонент. По найденным силам выполнен расчет усталостной прочности винтов при нагрузке на срез для каждой конфигурации артропластики. В окрестности каждого из фиксирующих винтов рассмотрены субмодели, учитывающие профиль резьбы, для получения уточненного напряженно-деформированного состояния вблизи винта. В отдельных точках на кромке резьбы рассчитаны коэффициенты интенсивности напряжений КИН, обусловленные появлением малой трещины в спонгиозной кости в окрестности вершины профиля резьбы. По найденным КИН вычислены возможные скорости роста усталостной трещины в кости на кромке резьбы на основе формулы Париса [15]. В процессе шага винт, который проводится из ацетабулярного компонента в передне-нижний квадрант вертлужной впадины (рис. 1), для пациентов групп 1 и 2, подвергается наибольшим растягивающим силам, именно этот винт следует признать наиболее слабым. Винты, установленные в верхние квадранты, на всех стадиях шага испытывают только сжимающие воздействия. Эти тенденции сохраняются во всех рассмотренных конфигурациях.

Рис. 1. Схема направления винтов, проводимых из ацетабулярного
компонента в кости таза
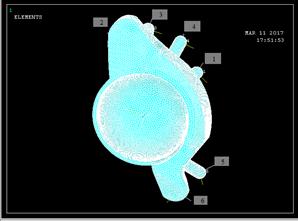
Рис. 2. Схема направления винтов, фиксирующих антипротрузионное кольцо
Кольцо Бурх-Шнайдера фиксируется в вертлужной впадине с помощью шести спонгиозных винтов, расположенных так, как показано на рисунке 2. На практике в КБШ устанавливается вкладыш цементной фиксации. В силу того что КБШ имеет отверстия, цемент может обеспечивать дополнительную фиксацию самому кольцу (рис. 3). Крепление кольца к поверхности кости в ANSYS моделируется уравнениями связи AdjacentRegion.
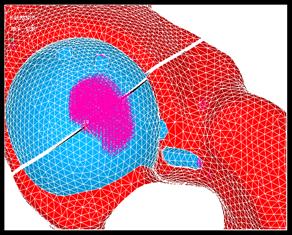
Рис. 3. Зона контакта цементной мантии КБШ и костей таза
В процессе шага винт 6 подвергается наибольшим растягивающим осевым нагрузкам и по этому формальному критерию должен быть признан наиболее опасным. Винты 1, 3, 4 на всех стадиях шага испытывают только сжимающие нагрузки (рис. 2). Длительная прочность винта 6 (имеет наибольшие растягивающие нагрузки) в конфигурации, рассмотренной в данной работе, формально обеспечивает число циклов, признанное достаточным для этапа первичной фиксации (9 х 105 при всех трех рассмотренных наборах параметров материала спонгиозной кости). Конфигурация с кольцом Бурх-Шнайдера является наиболее предпочтительной для создания первичной стабильности.
В проведенном исследовании, основываясь на публикациях в современной литературе, полученных клинико-функциональных, рентгенологических и статистических данных, а также анализе ошибок и осложнений, повлекших за собой развитие неудовлетворительных результатов лечения, проведенном математическом эксперименте, нами был сформулирован алгоритм выбора конструкции при эндопротезировании пациентов с последствиями сложных переломов вертлужной впадины.
В основе разработанного нами алгоритма выбора лежит рентгенологическая оценка исходного повреждения вертлужной впадины. Для проведения данной оценки целесообразно выполнение рентгенографии травмированного тазобедренного сустава в 2 стандартных проекциях (прямая и аксиальная проекции), однако рентген-снимки поврежденного сустава не дают полного представления об объеме дефектов и степени смещения отломков, поэтому обязательным является выполнение спиральной компьютерной томографии. Компьютерная томография с 3D-реконструкцией костей таза позволяет максимально объективизировать степень повреждения и характер смещения отломков.
На основании ретроспективных данных и их статистического анализа нами установлено, что наиболее оптимальным доступом при оперативном лечении пациентов с последствиями сложных переломов вертлужной впадины является задний доступ Кохера- Лангенбека к тазобедренному суставу, позволяющий хорошо визуализировать область вмешательства и осуществлять манипуляции, в связи с чем сокращается время операции. Продолжительность оперативного вмешательства при использовании заднего доступа короче, чем при использовании передне-наружного и комбинированного доступов (р= 0,001), в результате чего снижается кровопотеря. Так, наименьшая кровопотеря наблюдалась при использовании заднего доступа, в отличие от передне-наружного и комбинированного (р= 0,004). При клинико-рентгенологическом обследовании пациентов в послеоперационном периоде получены хорошие функциональные результаты.
По результатам математического расчета вариантом для создания первичной стабильности ацетабулярного компонента при тотальном эндопротезировании у пациентов с последствиями сложных переломов вертлужной впадины является способ артропластики с использованием антипротрузионного кольца Бурх-Шнайдера.
По нашему мнению, создание модульной системы (кольцо Бурх-Шнайдера + ацетабулярный компонент) при эндопротезировании тазобедренного сустава, у пациентов с исследуемой патологией, для создания первичной стабильности вертлужного компонента является предпочтительным направлением.
Разработанный алгоритм выбора способа оперативного лечения пациентов с последствиями сложных переломов вертлужной впадины позволяет определить хирургическую тактику с минимальными материальными затратами на предоперационное обследование. Данный алгоритм позволяет улучшить функциональные результаты эндопротезирования тазобедренного сустава у пациентов с исследуемой патологией.
Экономический фактор вместе с относительной простотой использования предложенного алгоритма позволяет рекомендовать его для практической работы травматологов-ортопедов.
ГУ Институт ортопедии и травматологии НАМН Украины
01054, Украина, г. Киев,
ул. Воровского, 27.
Контакты травматолога-ортопеда:
+38 067 963 2785 Моб.
+38 044 000 0000 Telephone:
+38 044 000 0000 FAX:
-->
Новые страницы:
-
2016.02.05 Необходимость фиксации малоберцовой кости при переломах костей голени 2015.07.02 Мультфильм ортопеды Киева, Украина 2014.10.29 Лечение вывиха грудинного конца ключицы 2014.10.29 Лечение вывиха акромиального конца ключицы 2014.10.29 Лечение переломов латерального конца ключицы 2014.10.29 Интрамедуллярный остеосинтез переломов ключицы 2014.10.29 Лечение переломов диафиза ключицы 2014.10.29 Лечение переломов ключицы и вывихов в прилежащих суставах 2014.10.29 Послеоперационное лечение переломов лопатки 2014.10.29 Хирургические доступы при лечении переломов лопатки
Лечение переломов вертлужной впадины
Лечение при изолированных переломах тела подвздошной кости, проникающих в вертлужную впадину, проводится путем разгрузки сустава применением системы постоянного скелетного или клеевого вытяжения в средне-физиологическом положении конечности в течение 4 нед.
Движения в суставе начинаются по стихании острого болевого синдрома (через 5—7 дней). Дотированную нагрузку разрешают через 4—5 нед, полную — через 8—10 нед. Трудоспособность восстанавливается через 10—12 нед. При чрезвертлужных переломах таза наступает угловое смещение отломков в сторону полости таза — диагональный размер входя в полость малого таза уменьшается. Репозиция отломков может быть достигнута методом постоянного скелетного вытяжения за конечность стороны повреждения. Спицу проводят за надмыщелки бедра, первоначальный груз 4 кг, сопоставление отломков обычно наступает при грузах 6—7 кг. Длительность вытяжения — 8 нед, через 2—3 нед с момента травмы начинается лечебная гимнастика для тазобедренного сустава. Дотированная нагрузка на конечность стороны повреждения возможна через 10—12 нед после травмы, полная — через 4—6 мес. Трудоспособность — через 5—7 мес.
При переломах дна вертлужной впадины без смещения головки накладывают систему постоянного скелетного вытяжения на 4 нед, лечебная гимнастика начинается с 3—4-го дня, дозированная нагрузка возможна через 8 нед после травмы, полная — через 12—14 нед. Трудоспособность восстанавливается через 4—5 мес.
При переломах дна вертлужной впадины со смещением головки в полость таза (центральный вывих бедра) репозиция достигается применением системы постоянного скелетного вытяжения: спицу проводят за надмыщелковую область бедра с первоначальным грузом на скелетной тяге 4 кг. Конечность укладывают в положении приведения и сгибания в тазобедренном и коленном суставах. Для устранения смещения головки проводят вытяжение по оси шейки с помощью петли на проксимальный конец бедра (при неглубоком внедрении головки) или скелетной тяги за область большого вертела с первоначальным грузом 4 кг. Наращивание грузов проводят вначале только по оси шейки бедра до устранения вывиха головки. После достижения вправления грузы постепенно переносят на скелетную тягу по оси конечности с оставлением первоначального груза по оси шейки. Конечность после достижения репозиции постепенно (в течение недели) отводится до угла 90—95°. Длительность вытяжения — 8—10 нед. Движения в суставе разрешаются спустя 1—2 нед по достижении репозиции. Дозированная нагрузка на конечность возможна через 2, 5—3 мес, полная — через 4—6 мес. Трудоспособность восстанавливается через 5—7 мес. При переломах задне-верхнего края вертлужной впадины без смещения головки (без смещения фрагмента) накладывают систему постоянного клеевого вытяжения на 4 нед. Движения в суставе начинаются со 2-й недели. Дозированную нагрузку разрешают через 6 нед, полную — через 8—10 нед.
Трудоспособность восстанавливается через 3 мес.
При переломах задне-верхнего края вертлужной впадины со смещением головки бедра (верхние и задние вывихи бедра) под общим обезболиванием проводят устранение вывиха. Если вправление устойчивое (по прекращении тракции по длине и проведении пассивных движений в суставе рецидив вывиха не наступает), осуществляется разгрузка сустава применением постоянного клеевого вытяжения в течение 4 нед в положении умеренного сгибания, отведения и наружной (при верхне-задних вывихах) или внутренней
Обычно устойчивая репозиция наблюдается при переломе небольшого фрагмента края вертлужной впадины, который не испытывает нагрузки и такой перелом носит отрывной характер. Поэтому после прекращения вытяжения больному разрешается дозированная нагрузка, а полная возможна через 6—8 над. Примерно в этот же срок восстанавливается трудоспособность.
Если вывих бедра сопровождается переломом большого фрагмента крыши вертлужной впадины, который находится в зоне нагрузки головки, положение головки бывает неустойчивым — вывих рецидивирует после прекращения тяги по длине и приведении бедра.
Лечебная тактика в таких случаях зависит от того, наступит ли репозиция костного фрагмента при вправлении головки бедра или фрагмент не сопоставится. Если при устранении вывиха достигается и сопоставление костного фрагмента, то стабилизация положения достигается применением системы постоянного скелетного вытяжения за надмыщелки бедра с применением удерживающих грузов (6—7 кг).
Длительность скелетного вытяжения — 6—8 нед. Затем в течение 2—4 нед осуществляется клеевое вытяжение с лечебной гимнастикой в тазобедренном суставе. Дозированная нагрузка возможна через 10—12 нед, полная — через 4—6 мес. Если при неустойчивом положении головки бедра не наступает сопоставление костного фрагмента, что наблюдается при ротационном характере его смещения, необходимо оперативное сопоставление фрагмента и фиксация его винтами, В послеоперационный период целесообразно проводить разгрузку сустава применением постоянного клеевого вытяжения в течение 6—8 нед с ранней лечебной гимнастикой. Дозированная нагрузка разрешается через 10—12 нед, полная — через 4—6 мес.

Авторами описаны атипичные переломы вертлужной впадины, а так же представлен рациональный алгоритм экспресс диагностики этих переломов. Представлены клинические примеры сопутствующих локальных повреждений.
Ключевые слова
Полный текст
Большинство переломов вертлужной впадины соответствует десяти основным типам согласно классификации R. Judet и E. Letournel [1, 2]. Однако существует ряд переломов, которые сложно отнести к какому-либо определенному типу, это обусловлено многообразием расположения плоскостей излома. Среди атипичных форм переломов можно выделить такие типы как Т-образный ассоциированный с переломом задней стенки, изолированный перелом четырехсторонней пластинки.
Алгоритм выявления атипичных форм идентичен таковому для ассоциированных типов — анализ обзорных рентгенограмм и детализация прицельных снимков. Для детализации очага повреждения мы выполняем прицельные рентгенограммы в подвздошной и запирательной проекции и КТ, что имеет решающее значение в детализации атипичных переломов. В конечном итоге полноценно проведенное лучевое обследование пациента позволяет выбрать оптимальный способ хирургической коррекции и операционный доступ.
Представляем клинические примеры атипичных переломов вертлужной впадины.
На обзорной рентгенограмме таза (рис. 1, а) определяется сочетание нарушений контуров трех линий (подвздошно-гребешковая, подвздошно-седалищная, контуры запирательного отверстия), характерное только для 3 типов ассоциированных переломов: Т-образного перелома, перелома передней колонны, ассоциированного с задним полупоперечным переломом, двухколонного перелома. Таким образом, на первом этапе из 10 возможных типов переломов, мы можем исключить 7 типов (рис. 1, а).
Целостность крыла подвздошной кости, как уже было отмечено ранее, позволяет исключить типы переломов, при которых наблюдается отдельный фрагмент передней колонны (перелом передней колонны, ассоциированный с задним полупоперечным переломом, двухколонный перелом). Таким образом, методом исключения диагностирован Т-образный перелом (рис. 1, в).

Рис. 1.а — обзорная рентгенография таза при поступлении; б — первый этап определения атипичного Т-образного перелома ассоциированного с переломом задней стенки; в — второй этап определения атипичного Т-образного перелома ассоциированного с переломом задней стенки; в — окончательное определение атипичного Т-образного перелома ассоциированного с переломом задней стенки; г, д, е, ж, з — детализация атипичного Т-образного перелома ассоциированного с переломом задней стенки с помощью прицельных рентгенограмм в подвздошной и запирательной проекциях и компьютерной томографии.
Однако при дальнейшем анализе обзорной рентгенограммы обращает на себя внимание отдельный фрагмент задней стенки. Соответственно в данном клиническом примере имеет место не Т-образный перелом, а атипичный Т-образный перелом, ассоциированный с переломом задней стенки (рис. 1, в).
Выполнение прицельных рентгенограмм и КТ позволяет подтвердить характер перелома. Как на рентгенограммах, так и на КТ отчетливо видна поперечно ориентированная линия перелома, проходящая через свод вертлужной впадины (транстектальный перелом), которая разделяет латеральные отделы тазового кольца на крыло и тело подвздошной кости и лобково-седалищный сегмент.
Рис. 2.а — обзорная рентгенография таза при поступлении; б — первый этап определения атипичного перелома четырехсторонней пластинки; в — окончательное определение атипичного перелома четырехсторонней пластинки; г, д — детализация перелома четырехсторонней пластинки с помощью прицельных рентгенограмм в запирательной и подвздошной проекции.
На прицельной рентгенограмме в запирательной проекции и КТ определяем отдельную плоскость излома, которая располагается в области задней стенки (рис. 1, д, з).
На рис. 1, ж видна вертикальная линия перелома, которая разделяет лобково-седалищный сегмент на передний и задний фрагмент (линия проходит через четырехстороннюю пластинку). Очень важно при планировании операции учитывать, что лобково-седалищный сегмент состоит из двух фрагментов.
В следующем клиническом примере на рентгенограмме таза в переднезадней проекции мы определяем целостность 4 основных референтных линий: подвздошно-гребешковая, подвздошно-седалищная, контуры запирательного отверстия, задняя стенка (рис. 2, а). На первом этапе диагностики мы исключили все возможные 10 типов по классификации Judet—Letournel, однако на рентгенограмме определяется центральное смещение головки бедренной кости и наличие отломков вне контуров референтных линий (рис. 2, б).
Обращает на себя внимание разрушение фигуры слезы. Анатомически это объясняется локализацией повреждения в передненижних отделах вертлужной впадины. Соответственно, хорошо различимые смещенные костные отломки представляют собой часть четырехсторонней пластинки, которая является дном вертлужной впадины (рис. 2, в).
Выполнение прицельных рентгенограмм позволяет нам подтвердить целостность анатомических структур, формирующих референтные линии (передняя и задняя колонны, края впадины). Наличие центрального вывиха головки бедренной кости характерно для переломов с поперечной линией излома, когда головка бедренной кости вклинивается между подвздошной костью и лобково-седалищным сегментом. В данном случае на рентгенограммах в подвздошной и запирательной проекции отчетливо определяется протрузия головки бедра в таз в проекции четырехсторонней пластинки, что подтверждает перелом дна вертлужной впадины (рис. 2, д).
Следует отметить, что повреждение четырехсторонней пластинки характерно для переломов на фоне остеопороза.
На обзорной рентгенограмме в следующем клиническом примере определяем целостность подвздошно-седалищной линии (рис. 3, а). Сохранение целостности этой структуры позволяет исключить переломы, при которых плоскость излома проходит через заднюю колонну. К этим переломам относят: перелом задней колонны, поперечный перелом, перелом задней колонны, ассоциированный с переломом задней стенки, поперечный перелом, ассоциированный с переломом задней стенки, Т-образный перелом, перелом передней колонны, ассоциированный с задним полупоперечным, двухколонный перелом (рис. 3, б).

Рис. 3.а — обзорная рентгенография таза при поступлении; б — первый этап определения атипичного внесуставного перелома передней колонны; в — второй этап определения атипичного внесуставного перелома передней колонны; г, д, е, ж — верификация внесуставного перелома передней колонны с помощью прицельных рентгенограмм в косой-подвздошной и косой-запирательной проекциях и компьютерной томографии.

Рис. 4.а, б — перелом вертлужной впадины слева; Ц — оскольчатый характер перелома задней стенки вертлужной впадины.
Сочетание повреждения подвздошно-гребешковой линии и контуров запирательного отверстия позволяет исключить перелом задней стенки, т.к. при подобных переломах сохраняется целостность обеих линий. Так же возможно исключить перелом передней стенки, при котором имеет место повреждение только подвздошно-гребешковой линии без повреждения контуров запирательного отверстия (рис. 3, в). Таким образом, методом исключения диагностирован перелом передней колонны.
Однако при наличии признаков перелома передней колонны, отсутствует повреждение суставной поверхности, что возможно подтвердить с помощью поли проекционной рентгенографии и компьютерной томографии. При анализе прицельных снимков видно, что линии перелома не проходят через суставную поверхность, что так же подтверждается на трехмерной компьютерной реконструкции костей таза (рис. 3, в—ж).
Исходя из результатов трехмерной реконструкции, наиболее подходящим диагноз можно сформулировать, используя классификации Л.Г. Школьникова (1966) или А.Ф. Лазарева (1992) [3, 4]. Согласно первой классификации этот перелом соответствует типу 3.В.б), т.е. перелом с нарушением непрерывности тазового кольца, как в переднем, так и заднем отделах.
Согласно второй классификации этот перелом относится к полифокальным повреждениям таза с вовлечением передних и задних отделов.
Наличие нескольких линий перелома не всегда свидетельствует об ассоциированном характере перелома (по классификации Judet—Letournel). Локализация этих линий может быть в пределах одной плоскости, что свидетельствует об оскольчатом характере перелома. На рентгенограммах (рис. 4, а, б) представлен пример оскольчатого перелома задней стенки вертлужной впадины.
При видимом наличии нескольких линий перелома, отмечается целостность других референтных линий, что свидетельствует о локализации очага повреждения только задней стенки (рис. 4, в, г).

Рис. 5. Импакция верхнее-медиальных отделов сурсила (Gull-sign).

Рис. 6.а—г. Наличие теней костной плотности в проекции суставной щели (внутрисуставные осколки); в, г — верификация наличия внутрисуставных осколков по данным КТ.
Сложность рентгенологической анатомии тазобедренного сустава значительно затрудняет выявление внутрисуставных отломков. Заподозрить наличие внутрисуставных осколков возможно при наличии теней костной плотности в проекции суставной щели как минимум в 2 проекциях (рис. 6, а—г).
Однако окончательная диагностика этого сопутствующего локального компонента повреждения возможна с помощью КТ (рис. 6д, е).
Переломы головки чаще встречаются при переломах вертлужной впадины с локализацией очага в задних отделах (задняя колонна, задняя стенка). Перелом головки довольно часто носит импрессионный характер и проявляется в виде участка вдавления верхнего полюса головки (рис. 7, а, б). Наиболее часто повреждения головки бедренной кости наблюдаются у пациентов старше 40 лет, что обусловлено снижением качества костной ткани.
В некоторых случаях импрессионных переломов головки рентгенография не является достаточно убедительной для верификации. Окончательное определение повреждения головки бедренной кости проводим по данным КТ (рис. 8, а, б). Сочетание перелома вертлужной впадины и нагружаемой части головки бедренной кости является крайне неблагоприятным прогностическим признаком.

Рис. 7. Импрессионный перелом головки в сочетании с переломом задней колонны (а, б).

Рис. 8. Импрессионный перелом головки бедренной кости по данным КТ при отсутствии признаков повреждения головки по данным рентгенографии (а, б).
Заключение. Атипичные переломы невозможно причислить к какому-либо из 10 типов переломов по классификации Judet—Letournel. Знание нормальной рентгенологической анатомии вертлужной впадины позволяет определить локализацию и характер очагов при этих сложных повреждениях. Определение сопутствующих локальных повреждений играет значительную роль для выбора тактики лечения.
У 13 взрослых беспородных собак моделировали центральный поперечный перелом вертлужной впадины с последующей репозицией отломков и поддержанием их стабильной фиксации аппаратом Илизарова. Патоморфологическое исследование седалищного нерва через 14 и 42 суток лечения перелома методом чрескостного остеосинтеза обнаружило травматизацию нерва по типу нейропраксии и аксонотмезиса. В 23,1 % случаев доля измененных волокон не превышала 5 %. У 53,8 % собак обнаруживались признаки нарушения эпиневральной и эндоневральной васкуляризации нерва, признаки реактивного воспаления эпиневрия, периневрит и значительная, до 20 %, травматизация нервных проводников. В 15,4 % случаев аксональная и валлеровская дегенерация охватывала более 20 %-30 % волокон, и у 7,7 % собак она приобретала массовый характер.

1. Булибина Т. Восстановительное лечение невропатий седалищного нерва при переломах вертлужной впадины // Врач. – 2006. – № 5. – С. 65-67.
2. Варсегова Т.Н., Краснов В.В. Морфологическое исследование седалищного нерва при лечении сочетанной травмы таза и бедра методом чрескостного остеосинтеза в эксперименте // Гений ортопедии. – 2010. – №4. – С. 36-40.
3. Зубарева Т.В., Стэльмах К.К., Шлыков И.Л. Особенности нервно-мышечного аппарата у больных с переломами костей таза в поздние сроки после травмы // Травматология и ортопедия России. – 2006. – № 2 (40). – С. 127-128.
4. Смирнов А.А., Павлов Д.В., Варварин О.П. Хирургическая тактика при переломах вертлужной впадины // Травматология и ортопедия России. – 2009. – № 4 (54). – С. 84-87.
5. Структурная реорганизация малоберцового нерва при заживлении переломов костей голени в эксперименте / Т.Н. Варсегова, Н.А. Щудло, М.М. Щудло, Н.В. Петровская, М.А. Степанов // Успехи современного естествознания. – 2013. – № 6. – С. 13-18.
6. Щеткин В.А., Пузин С.Н., Якимов С.А. Медико-социальные последствия переломов и переломовывихов вертлужной впадины // Медико-социальная экспертиза и реабилитация. – 1999. – № 2. – С. 32-35.
7. Щудло М.М. Рост и дифференцировка структур эпи-периневрия в условиях дозированного растяжения // Вестник РАМН. – 2000. – № 2. – С. 19-23.
8. Iatrogenic nerve injury in acetabular fracture surgery: a comparison of monitored and unmonitored procedures / G.J. Haidukewych, J. Scaduto, D.Jr. Herscovici, R.W. Sanders, T. Di Pasquale // J. Orthop. Trauma. – 2002. – № 16 (5). – Р. 297-301.
9. Mortality in patients with pelvic fractures: results from the German pelvic injury register / O. Hauschild, P.C. Strohm, U. Culemann, T. Pohlemann, N.P. Suedkamp, W. Koestler et al. // J. Trauma. – 2008. – V. 64, № 2. – Р. 449-455.
10. Quan D., Bird S.J. Nerve Conduction Studies and Electromyography in the Evaluation of Peripheral Nerve Injuries // The University of Pennsylvania Orthopaedic Journal. – 1999. – № 12. – Р. 45–51.
Рост тяжелого травматизма в последние годы привел к увеличению числа пострадавших с повреждениями тазобедренного сустава [6], наиболее частыми из которых являются переломы вертлужной впадины [4], составляющие по разным источникам у взрослого населения 3-8 % от переломов костей таза [9]. Они происходят главным образом в результате высокоскоростной травмы при дорожно-транспортном происшествии либо падении с высоты и чаще встречаются у молодых людей и трудоспособной части населения [4], что определяет социально-экономическую значимость данной проблемы.
Трудность лечения больных с последствиями таких переломов определяется сопутствующей травматизацией органов малого таза, повреждением нервных стволов и сплетений [3]. Неврологический дефицит в виде частичного или полного пареза седалищного нерва наблюдается у 7,9-24,6 % больных [1, 4, 8]. Седалищные невропатии, связанные с травмой таза, в том числе переломом вертлужной впадины, распознаются, как правило, в поздние сроки лечения [3], что диктует необходимость ранней диагностики характера и степени тяжести повреждения седалищного нерва с целью выбора адекватных методов реабилитационной терапии.
В ранее проведенных исследованиях изучено изменение седалищного нерва при сочетанном переломе седалищной кости и шейки бедренной кости [2]. Сведения об этиопатогенезе седалищных невропатий при переломах вертлужной впадины, необходимые для решения лечебно-тактических вопросов, в доступной литературе не найдены.
Цель исследования – выявить патоморфологические изменения седалищного нерва при лечении перелома вертлужной впадины методом чрескостного остеосинтеза в эксперименте.
Материалы и методы исследования
Результаты исследования и их обсуждение
У всех животных в течение всего эксперимента седалищный нерв на стороне повреждения сохранял анатомическую непрерывность.
Через 14 и 42 суток лечения в седалищных нервах наблюдались аналогичные патоморфологические изменения.
У 3 собак в изученные сроки лечения перелома (14 и 42 суток) доля деструктивно измененных волокон с признаками демиелинизации, аксональной и валлеровской дегенерации не превышала 5 % (в интактном седалищном нерве этот показатель составил 2,51±0,1 %). У этих животных седалищный нерв отличался от аналогичного интактного нерва незначительно. Соединительнотканные оболочки нерва сохраняли целостность. В эпиневрии повышалось количество фибробластов, фиброцитов и тучных клеток. Вблизи эпиневральных сосудов располагались периваскулярные клетки, единичные макрофаги и плазматические клетки. Эпиневральные сосуды имели расширенные просветы, ядра эндотелиальных клеток кубической или округлой формы выбухали в просвет. Средняя оболочка была утолщена. Через 42 суток лечения наблюдалась незначительная гиперваскуляризация эпиневрия. Периневрий сохранял целостность и типичное для неповрежденного нерва строение. Между слоями периневральных клеток формировались многочисленные поперечные мостики (рис. 1А), представленные цитоплазматическими клеточными выростами. Признаки субпериневральных отеков не обнаруживались. Эндоневральные кровеносные сосуды сохраняли нормальное строение, но имели, в отличие от интактного нерва, расширенные просветы. Большинство (95 % и более) миелиновых нервных волокон имели нормальную структуру (рис. 1Б).
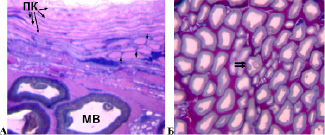
У 7 собак в течение эксперимента доля деструктивно измененных волокон с признаками демиелинизации, аксональной и валлеровской дегенерации составила в седалищном нерве 5-20 %. Соединительнотканные оболочки нерва сохраняли целостность. Эпиневрий выглядел отечным. Отмечалось повышение количества периваскулярных клеток, тучных клеток, которые в интактных седалищных нервах единичны. Появлялись отсутствующие в норме плазмоциты и лимфоциты. Визуально отмечалось повышение толщины стенок эпиневральных кровеносных сосудов относительно аналогичных микрососудов интактных нервов. Наружные оболочки большинства артерий и артериол были склерозированы. Часть мелких сосудов имела некротические изменения клеточных элементов стенки. Периневрий сохранял тонколамеллярное строение, часть периневральных клеток имела вакуолизированную цитоплазму. В отдельных пучках наблюдались периневральные (рис. 2 А) и субпериневральные отеки. Просветы эндоневральных микрососудов, в отличие от интактных нервов, были расширены. В эндоневрии отмечалось повышение относительно контроля количества фибробластов, фиброцитов, тучных клеток и нейролеммоцитов. Обнаруживались отсутствующие в контроле макрофаги и плазматические клетки. И в продольных, и в поперечных срезах были видны деструктивно измененные волокна (рис. 2 Б), однако большинство нервных проводников имели нормальную структуру.
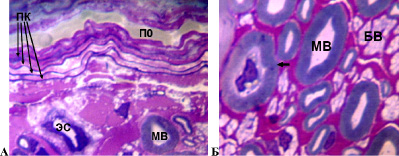
Рис. 2. Срок опыта 14 суток. А – периневрий, Б – нервные волокна седалищного нерва собаки. ПК – слои периневральных клеток. ПО – периневральный отек; ЭС – эндоневральный сосуд; МВ – миелиновое нервное волокно; БВ – безмиелиновое нервное волокно; стрелка – МВ с признаками аксональной дегенерации. Поперечный полутонкий срез. Окраска метиленовым синим и основным фуксином. Об. 100, ок. 12,5х
У 3 собак доля деструктивно измененных волокон в седалищном нерве составила более 20 %. При этом соединительнотканные оболочки нерва сохраняли целостность. Эпиневрий был отечным с признаками реактивного воспаления. В нерве обнаруживались скопления фибробластов, фиброцитов, тучных клеток (единичных в контроле), плазмоцитов и клеток лейкоцитарного ряда (в основном лимфоцитов). Визуально отмечалось повышение толщины всех слоев сосудистых стенок артерий и артериол эпиневрия в сравнении с контролем. Часть мелких сосудов имела некротические изменения клеточных элементов стенки. Периневрий утрачивал тонколамеллярное строение, большинство периневральных клеток имели вакуолизированную цитоплазму (рис. 3 А), обнаруживались обширные периневральные и субпериневральные отеки. Эндоневральные сосуды имели расширенные просветы, часть из них – признаки некротических изменений клеточных элементов стенки (рис. 3 Б). В поперечных и продольных срезах среди миелиновых волокон нормальной структуры были видны многочисленные проводники с признаками деструктивных изменений, продукты их распада, тучные клетки, нейролеммоциты, макрофаги и клетки воспалительного ряда. У одной собаки миелиновые волокна нормальной структуры были единичны (рис. 4).
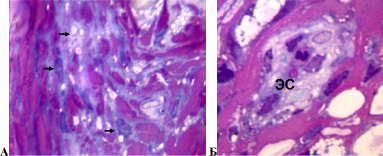
Рис. 3. Срок опыта 14 суток. А – периневрий, Б – эндоневральный микрососуд седалищного нерва собаки. Стрелками показаны периневральные клетки с вакуолизированной цитоплазмой. ЭС – эндоневральный сосуд с некротически измененными клеточными элементами всех слоев сосудистой стенки. Поперечный полутонкий срез. Окраска метиленовым синим и основным фуксином. Об. 100, ок. 12,5х
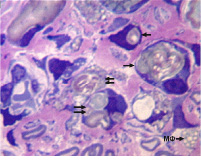
Рис. 4. Срок опыта 14 суток. Седалищный нерв собаки. Валлеровская дегенерация (стрелки) и продукты распада миелиновых волокон (двойные стрелки). МФ – макрофаги, содержащие крупные вакуоли. Поперечный полутонкий срез. Окраска метиленовым синим и основным фуксином. Об. 100, ок. 12,5х
Таким образом, у 23,1 % собак через 14 и 42 суток лечения перелома наблюдались умеренные реактивные изменения седалищного нерва, выражающиеся в повышении клеточности эпиневрия и его гиперваскуляризации к концу эксперимента, в изменении клеточных компонентов периневрия, аналогичных описанным при дистракционном остеосинтезе [7] и оскольчатом переломе голени собак [5]. Доля деструктивно измененных миелинизированных волокон не превышала 5 %.
У большинства исследованных животных даже при отсутствии механического повреждения оболочек седалищного нерва обнаруживались признаки нарушения эпиневральной и эндоневральной васкуляризации, признаки реактивного воспаления эпиневрия, периневрит и значительная травматизация нервных проводников. В 53,8 % случаев деструкции были подвержены до 20 % нервных проводников. По данным D.Quan, S.J.Bird (1999) при таком количестве травмированных аксонов восстановление нерва обеспечивается за счет терминального спраутинга интактных аксонов в срок от 2 до 6 месяцев. У 23,1 % животных аксональная и валлеровская дегенерация охватывала более 20 % волокон. При такой потере волокон коллатеральный спраутинг интактных аксонов и регенерация аксонов от места травмы становятся равнозначными механизмами восстановления нерва, на которое требуется от 2-6 до 18 месяцев [10].
Заключение. При переломе вертлужной впадины происходит травматизация седалищного нерва по типу нейропраксии и аксонотмезиса. При этом повреждаются миелиновые оболочки и аксоны нервных волокон с последующей валлеровской дегенерацией без поражения оболочек нерва, что может быть обусловлено его альтерацией в момент костной травмы и последующим сдавлением в травмированной области гематомами и формирующимися рубцово-спаечными образованиями. Несмотря на созданные благоприятные биомеханические условия для сращения отломков вертлужной впадины, в большинстве случаев, на морфофункциональное восстановление седалищного нерва, требуется не менее 6-18 месяцев.
Полученные экспериментальные данные послужат теоретическим обоснованием для разработки комплекса лечебных мероприятий при посттравматических невропатиях седалищного нерва, осложняющих переломы вертлужной впадины.
Читайте также:

